基准医疗-最新凯时注册
2017-05-12 来源:基准医疗
肿瘤形成之前就已开始转移的现象困扰科研人员已久。近期由美国西奈山伊坎医学院、爱因斯坦医学院、德国雷根斯堡大学等单位组成的研究团队发现,在肿瘤早期,具有特定分子变异的乳腺癌细胞就已经可以扩散到其他靶器官中,并长时间保持沉默,在特定条件下被激活,形成转移。相关成果被发表在顶级杂志《nature》上。
该研究虽揭示了肿瘤早期转移的机制,但却给医学界抛出另一个难题:既然早期肿瘤既已存在远处转移,势必会对患者手术效果及预后产生极大影响,因此早期追踪转移灶或术后监测残留病灶就显得尤为重要。最近基准医疗与福瑞德哈金森肿瘤医院中心的一项研究证实dna甲基化在前列腺癌术后复发风险预测中具有较高的应用潜力,相关研究成果发表在《clinical cancer research》。
一、肿瘤早期转移机制研究
该研究显示,在小鼠的早期病变及在检测到任何明显的原发肿块之前,有一种亚型为her2 p-p38lop-atf2lotwist1hie-cadlo的肿瘤细胞就已经发生扩散。活体成像和早期组织学病变研究发现her2 edccs局部侵入,并寄宿在靶器官。her2 edccs激活wnt依赖性上皮-间质转化(emt)程序,但没有完全丧失上皮表型。edccs表现为twist1hie-cadlo并潜伏,最终导致转移。该研究发现了一种肿瘤早期转移机制:her2能异常活化一个类似乳腺导管分支产生edccs的程序,从而在休眠期后形成转移。
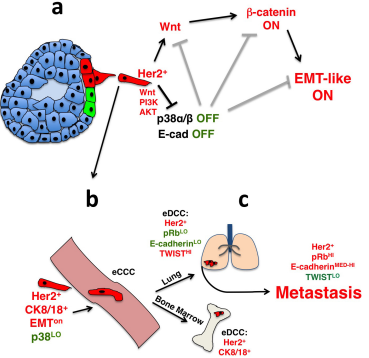
a、早期her2 癌细胞(红色)打开wnt、pi3k和akt信号通路,抑制p38的激活和e-cad的形成。p38和e-cad可抑制wnt和β-catenin驱动的emt样程序和侵袭(灰色抑制符号);
b、her2 p-p38lotwist1hie-cadlo早期癌细胞,仍表达ck8/18,并可侵入血管并传播;
c、肺组织中超过85%的edccs(红色)表现为her2 e-cadlo(p-rb和p-h3)lo,提示含大量的休眠细胞。多数edccs也表现为twist1hie-cadlo。然而edccs可以启动转移,这与获得twist1loe-cadmed–hi显性有关。在骨髓中,edccs表现为 her2 ck8/18 ,并保持持续休眠,而在骨病变并未观察到。
二、dna甲基化在前列腺癌术后复发风险预测中的研究
试验入组了来自该研究中心的430个手术切除的前列腺癌肿瘤组织,进行基因组范围的dna甲基化模式检测。转移灶则通过骨扫描,mri,ct,组织活检等结果进行确认。
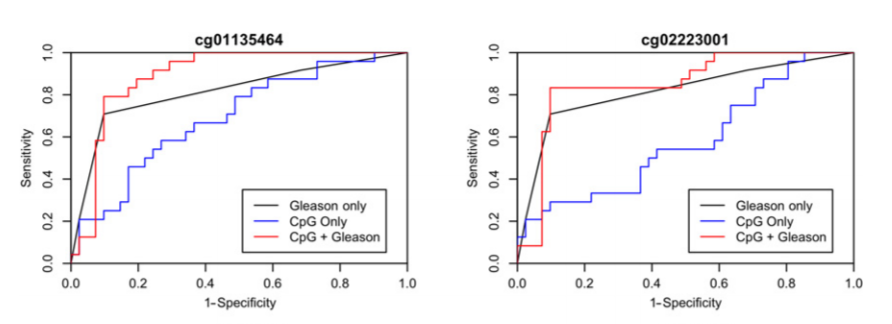
该研究鉴定出了一组新的可用于预测前列腺癌患者术后复发的dna 甲基化marker,并且能够显著提升gleason分级指数用于预测转移致死患者的能力。临床大样本试验结果显示dna甲基化在前列腺癌术后复发风险预测中的应用价值。
参考文献
[1]kathryn l. harper, maria soledad sosa, david entenberg, hedayatollah hosseini et al. mechanism of early dissemination and metastasis in her2 mammary cancer. nature, 22/29 december2016|vol540;
[2]zhao s, geybels m s, leonardson a, et al. epigenome-wide tumor dna methylation profiling identifies novel prognostic biomarkers of metastatic-lethal progression in men diagnosed with clinically localized prostate cancer[j]. clinical cancer research, 2017, 23(1): 311-319.

